こんにちは。化工見習いです!
今回は、「超臨界流体」と「臨界点」について簡単に紹介したいと思います。
超臨界流体、臨界点とは
超臨界流体とは、「液体と気体の区別がつかない状態」のことで、臨界点とは、物質がその「超臨界状態」になる温度、圧力のことを指します。
では、「液体と気体の区別がつかない状態」とはどういうことか説明していきます。イメージしてください。
①真空の箱(容積一定)に水を入れる
②常温で放置する
この時点で、水は液体の蒸気圧と、気体の圧力が等しくなるまで蒸発を続け、いずれ平衡点で釣り合います。
③温度を上昇させる
すると温度上昇に伴い、液体の蒸気圧の方が指数関数的に増大するので、これに追いつこうと、液体はどんどん蒸発していきます。
これを繰り返すと、水蒸気(気体)の密度はどんどん大きくなり、逆に水(液体)の密度はどんどん小さくなります。(補足あり)
最終的には水蒸気(気体)と水(液体)の密度が等しくなり、気体と液体の区別がつかなくなります。
この時の温度を臨界温度、圧力を臨界圧力といい、この状態を超臨界流体といいます。
補足
温度を上昇させると気体の密度が大きくなるのはなぜか
基本的に、液体の密度>気体の密度です。密度の高い液体が気体へ変わるので、気体全体の密度は大きくなります。
温度を上昇させると液体の密度が小さくなるのはなぜか
体積可変の容器に気体を入れて、温度を上昇させれば気体の密度は下がるのと同様で、分子運動が激しくなり、分子同士の距離が拡がっていくので、液体の密度も小さくなります。
状態図で見る
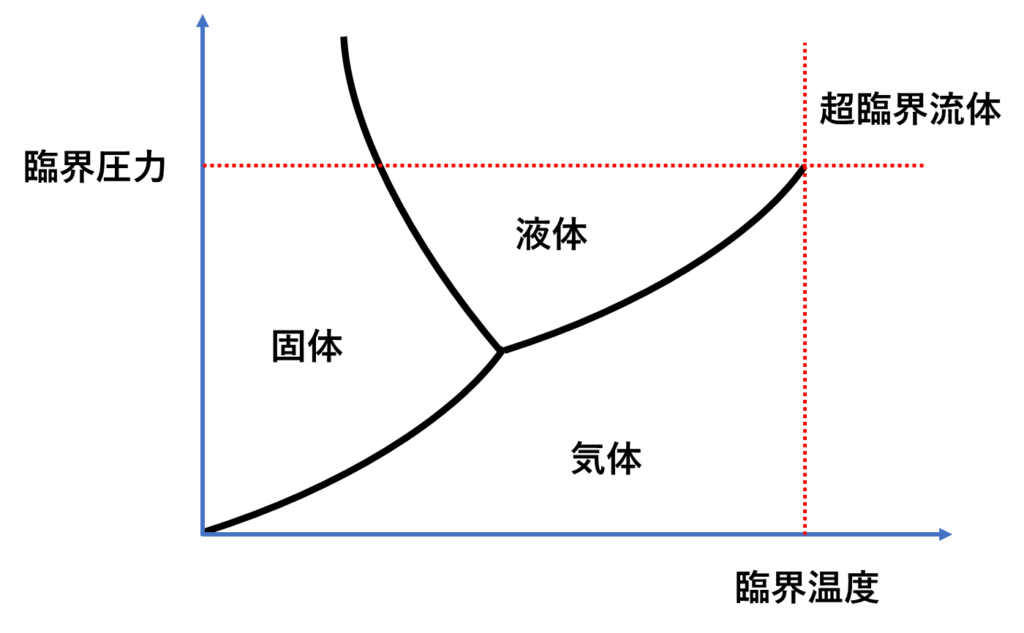
お馴染み「状態図」で超臨界流体を見てみます。
固体、液体、気体はそれぞれ昇華曲線、融解曲線、蒸発曲線によって区切られていますが、
超臨界流体はそのような曲線による状態の区切りはありません。臨界温度・臨界圧力以上の状態が「超臨界流体状態」となります。
また、この状態図を見ても分かる通り、
・臨界温度以上でも、臨界圧力以下であれば気体状態
・臨界圧力以上でも、臨界温度以下であれば液体状態
となります。高圧ガス資格なんかではこれについて問われることがたまにあります。
その他の特徴、用途
超臨界流体は、気体と液体の中間に位置しているようなもので、気液両方の性質を持っています。
つまり、圧力や温度の調整により、密度や粘度などの物性値を幅広く変化させることができるということです。
この性質を活かして、様々な物質を溶かしたり、クロマトグラフィーの移動相の溶媒として用いられたり、反応速度増加が期待できたり、といくつもの適用先があります。
まとめ
超臨界流体とは「気体と液体の区別がつかない流体」で、その中間的な性質により、化学実験や工業的に幅広く利用されています。
今回も最後まで読んでいただき、ありがとうございました。









